Кривая ликвидус на диаграмме состояния Мn–С в координатах концентрация углерода (ат. доли) – температура может быть выражена уравнением: lg[С] = –375,8/Т – 0347. Зависимость ∆G
6.1. Свойства марганца и его соединений |
Содержание > ГЛАВА 6. Электрометаллургия марганцевых ферросплавов > 6.1. Свойства марганца и его соединений
Марганец – элемент VIIb группы Периодической системы элементов Д.И.Менделеева*. Порядковый номер марганца 25, атомная масса 54,93, конфигурация внешней электронной оболочки атома 3d54s2, степень окисления от 2 до 7, наиболее устойчивы Mn(II) и Mn(IV). Известны четыре кубические кристаллические модификации марганца: ниже 727оС устойчива а = 0,89124 нм, z = 58, плотность 7,44 г/см3, при 727–1090оС – β-Mn (а = 6300 нм, z = 20, плотность 7,29 г/см3), при 1090–1138оC – γ-Mn (а = 0,38550 нм при 1100оС, z = 4, плотность 6,37 г/см3), выше 1138оС – δ-Mn (а = 0,30750 нм при 1143оС, z = 2, плотность 6,28 г/см3). Температура плавления 1244оС. Марганец имеет аномально высокую упругость пара. Зависимость давления пара марганца от температуры в интервале 1245–1545оС описывается уравнением:
lgPMn(Па) = 10,8828 – 13625/Т (1043 ≤ Т ≤ 1158 K)
lgPMn(Па) = 20,005 – 14850/Т + 2,52lgT (1517 ≤ Т ≤2353 K).
Система Mn–Fe(рис. 6.1). В системе Mn–Fe существует большая область твердого раствора на основе γ–Fe и γ–Mn. Растворы на основе α-Mn и β-Mn образуются при концентрации >68–70%Mn.
Низкая температура плавления сплавов в системе Mn–Fe составляет 1232оС при атомном содержании марганца 87%.
Интегральная энтальпия смешения достигает максимума –8360 Дж/моль при хMn = 0,7.
Система Mn–C (рис. 6.2). В системе идентифицированы следующие карбиды: Mn23C6 (5,38% C), Mn3C (6,77% C), Mn5C2 (8,03% C), Mn7C3 (8,57% C).
Кривая ликвидус на диаграмме состояния Мn–С в координатах концентрация углерода (ат. доли) – температура может быть выражена уравнением: lg[С] = –375,8/Т – 0347. Зависимость ∆G![]() (T) для реакции растворении графита в жидком марганце Ст + Мnж = [C]Mn имеет вид:
(T) для реакции растворении графита в жидком марганце Ст + Мnж = [C]Mn имеет вид:
∆G![]() = 17600 – 25,64Т, Дж/моль.
= 17600 – 25,64Т, Дж/моль.
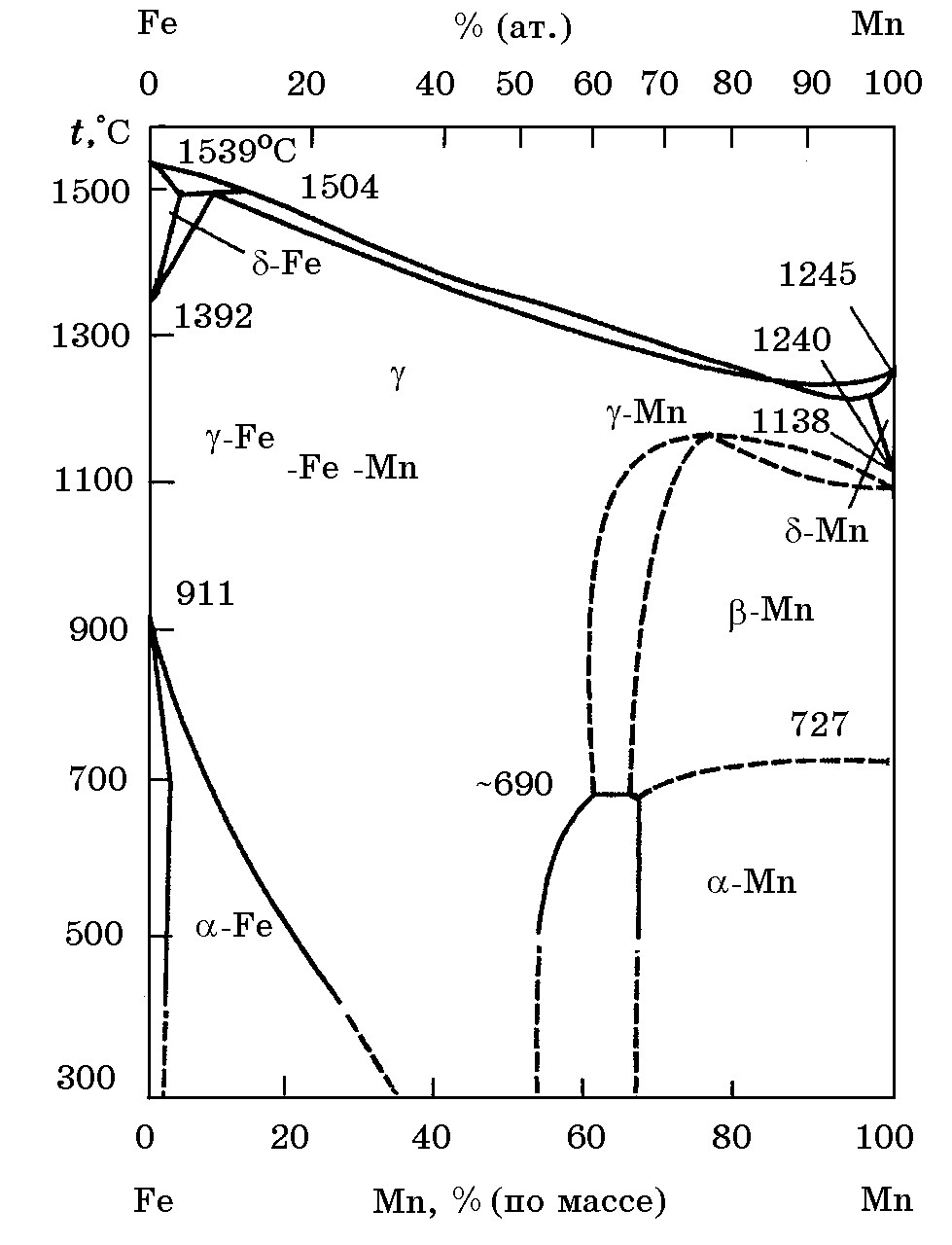
Рис. 6.1. Диаграмма равновесного состояния системы Fe–Mn
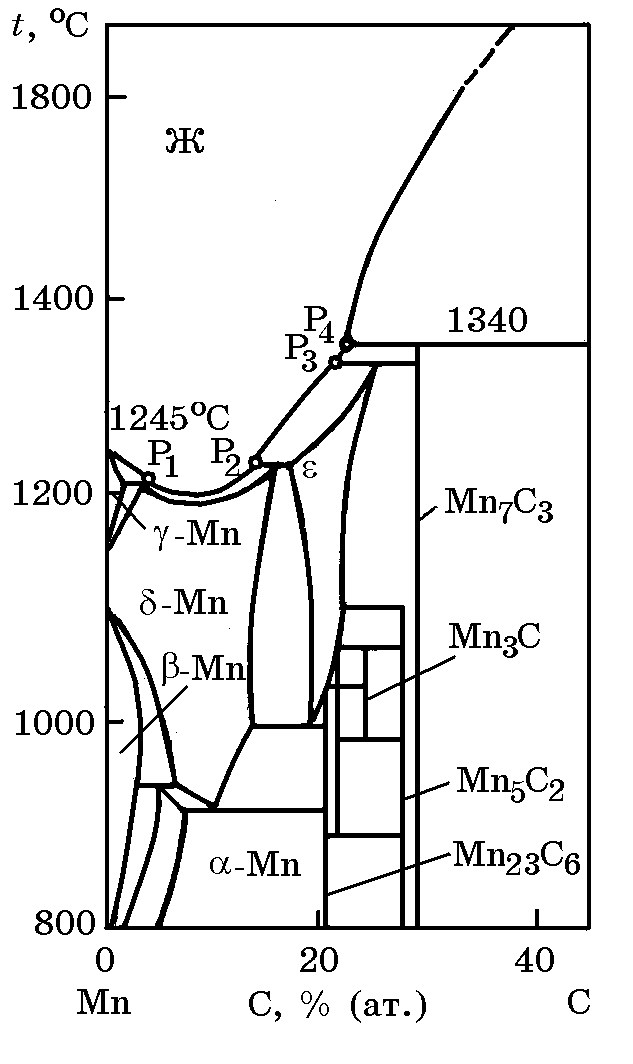
Рис. 6.2. Диаграмма равновесного состояния системы Mn–C
Зависимость изменения энергии Гиббса реакции образования высшего карбида марганца Мn7С3 из элементов 7Мn + 3С = Мn7С3 от температуры в интервале 1000-1150 K описывается уравнением:
∆Gо =66155 – 58,24Т, Дж/моль.
Система Mn–Si (рис. 6.3). Диаграмма состояния системы построена с учетом существования 7 силицидов марганца и твердых растворов кремния в марганце.
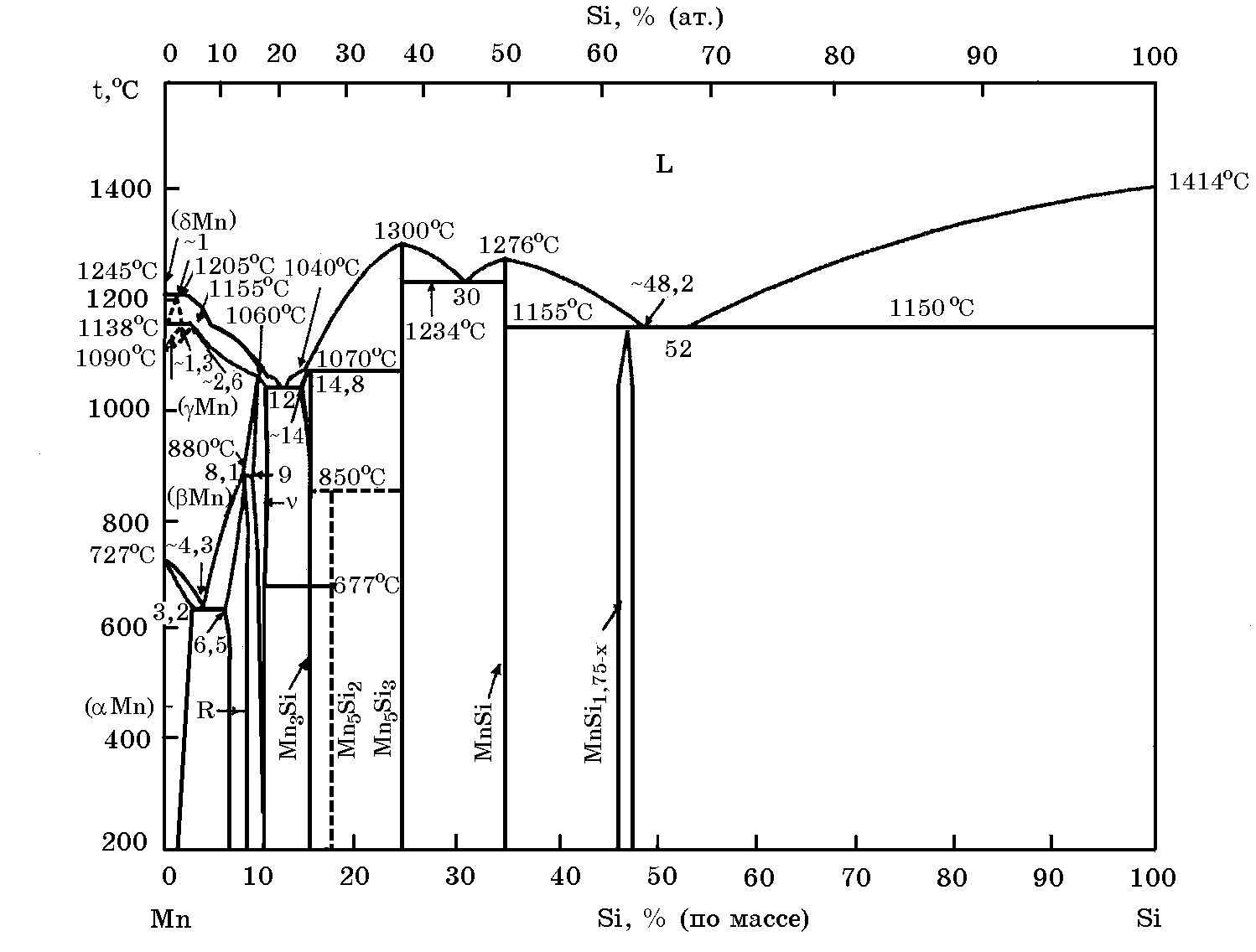
Рис. 6.3. Диаграмма равновесного состояния системы Mn-Si
Теплоты образования силицидов марганца Мn3Si, Мn5Si3, МnSi, МnSi1,7 соответственно равны 17; 24,85; 30,5 и 28,15 кДж/моль. Плотность жидких сплавов системы Мn–Si с повышением концентрации кремния уменьшается. При 1500 K и содержании кремния 30% и 60% (ат.) плотность сплавов составляет 5,31 и 4,35 г/см3 (6,37 и 2,32 г/см3 для чистых марганца и кремния).
Активность марганца и кремниz в расплавах Мn–Si зависит от состава сплава и температуры. Кривые аMn и аSi (рис. 6.4) пересекаются.
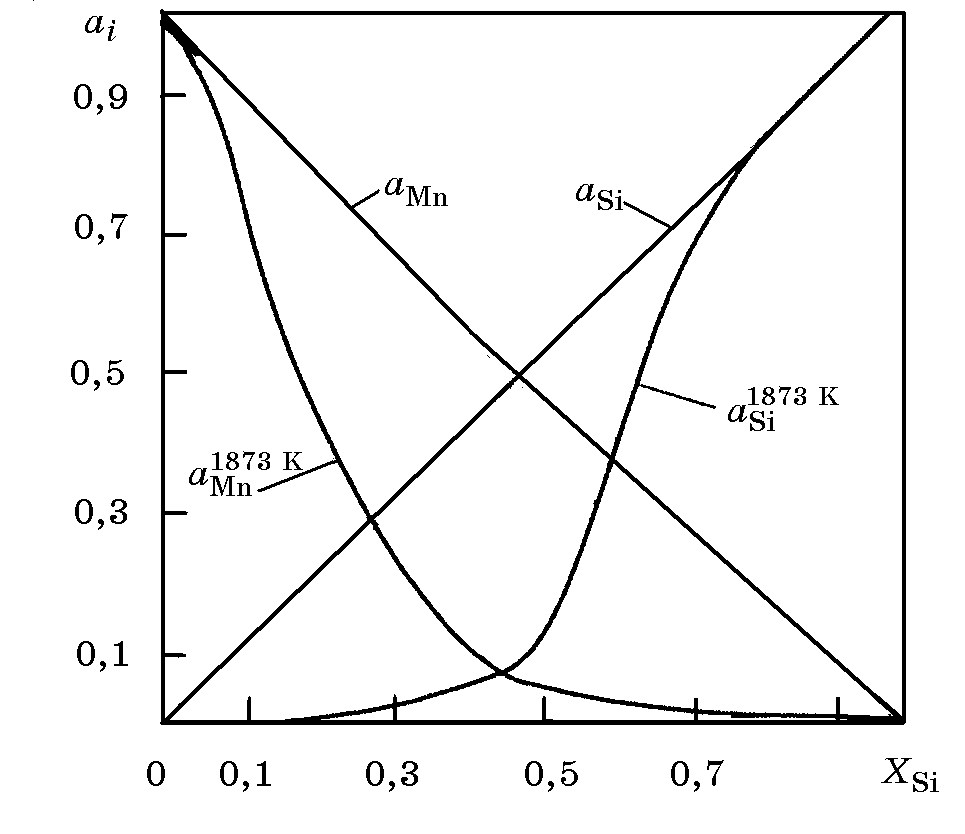
Рис. 6.4. Активность марганца и кремния в сплавах системы Mn–Si
при 1873 K (аMn и aSi – для гипотетического идеального, а1600Mn и а1600Si – для модельного растворов)
Структурными единицами расплавов системы Mn–Si в аспекте модели ассоциированных растворов* приняты Mn, S и три ассоциата Mn3Si, Mn2Si и MnSi. С помощью оптимизационной процедуры Б.М. Могутновым и др. (Россия) рассчитаны значения энтальпии и изменение энтропии, сопровождающие процессы ассоциации в системе Mn–Si (рис. 6.5):

Как следует из данных рис. 6.5, наибольшую долю в расплавах Mn–Si при 1873 K представляют ассоциаты MnSi.
Система Mn–Si–C(рис. 6.6). Растворимость и активность углерода в расплавах системы Mn–Si–C снижается по мере повышения содержания кремния, что объясняется более высокой термодинамической прочностью химических связей атомов марганца с кремнием, чем с углеродом**.
Это положение является общим для расплавов систем Fe–Si–C, Mn–Si–C и Cr–Si–C, а также для расплавов систем (Mn, Fe)–Si–C, (Cr, Fe)–Si–C и (Cr, Mn)–Si–C. На рис. 6.7 представлены криволинейные зависимости равновесных содержаний углерода в расплавах системы Mn–Si–C (кривая 1), системы (Mn, Fe)–Si–С (кривые 2, 3 и 4) и системы Fe–Si–C (кривая 5) при 1600оС.
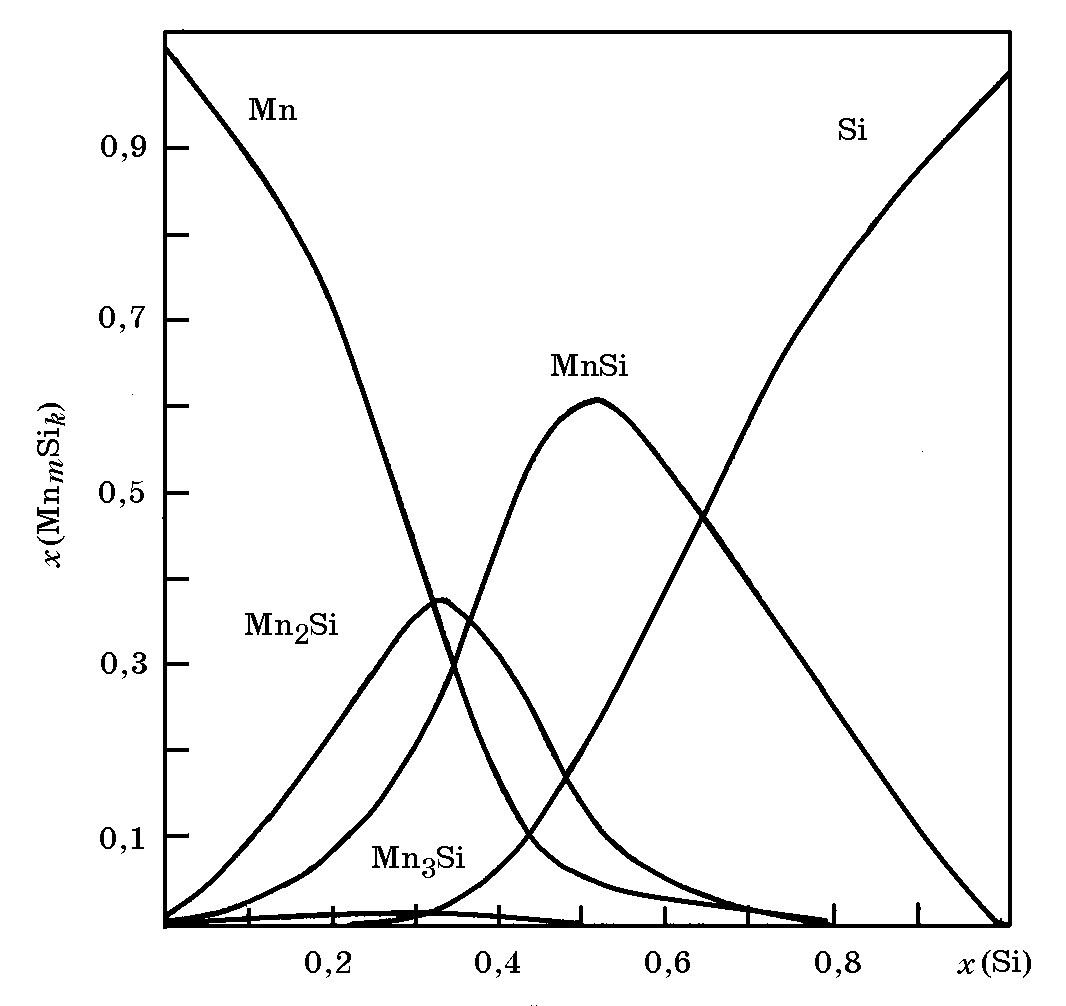
Рис.6.5. Силикокарбидные фазы в системе Mn–Si–C
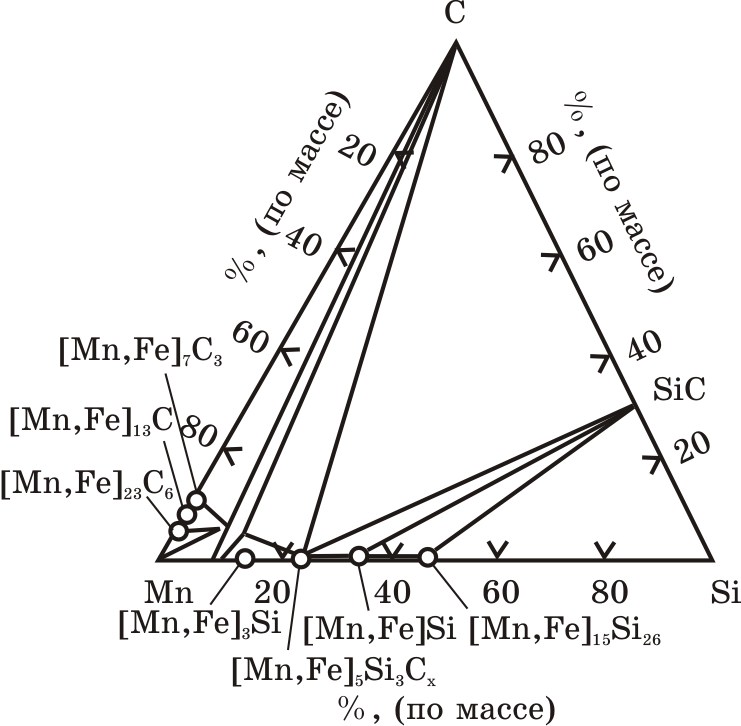
Рис. 6.6. Диаграмма равновесного состояния системы Mn–Si–C
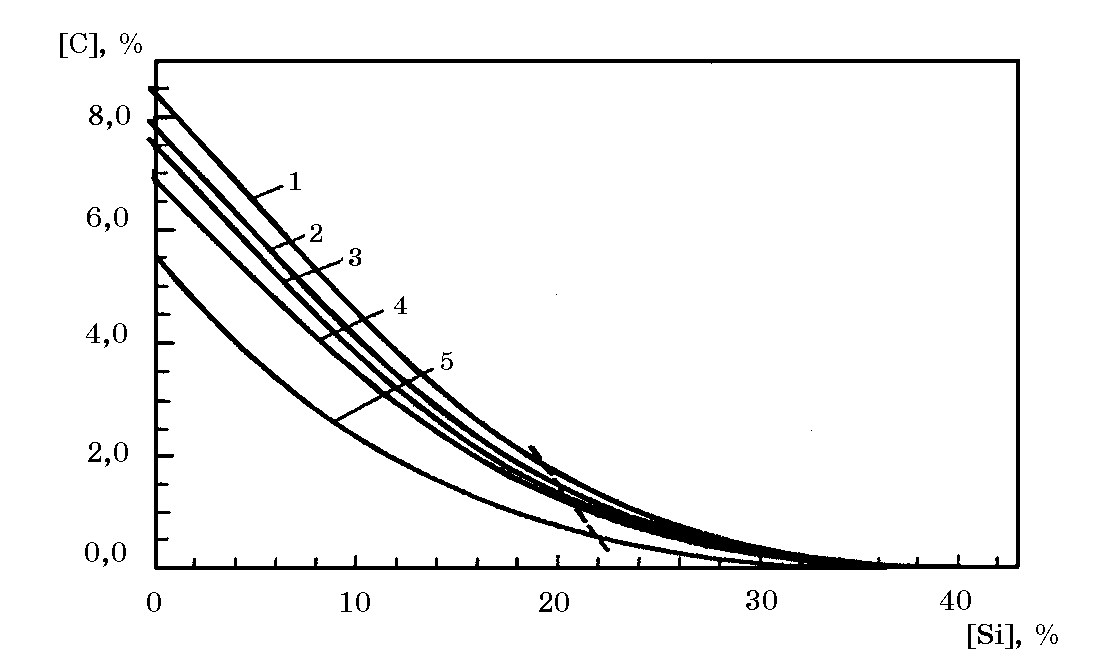
Рис. 6.7. Равновесные содержания углерода в зависимости от концентрации кремния в системах: 1 – Mn-Si-Cнас; 2 – Mn–Fe–Si–Cнас при %Mn/%Fe = 4; 3 – Mn–Fe–Si–Cнас при %Mn/%Fe = 2;
4 – Mn–Fe–Si–Cнас при %Mn/%Fe = 1; 5 – Fe–Si–Cнас
Наиболее высокая растворимость углерода имеет место в системе Mn–Si–C, наиболее низкая в системе Fe–Si–C. По мере уменьшения отношения %Mn/%Fe равновесная растворимость углерода уменьшается. Существенное различие в растворимости углерода в рассматриваемых системах при содержании кремния до ~10–15%, постепенно уменьшается, и свыше 23-25% кривые сливаются. Важно отметить, что при увеличении содержания кремния до 23–25% равновесной фазой является графит. В концентрационной области содержания кремния более 23–25% расплавы находятся в равновесии с карбидом кремния. Для системы Mn–Si–C предельным значением содержания кремния, при котором углерод может сосуществовать с карбидом кремния, является 23,48% Si, что соответствует составу фазы Новотного (Mn5Si3Cx).
В торговых марках ферросиликомарганца в зависимости от марки сплава может содержаться до 15-20% Fe при 65% Mn. На рис. 6.8 представлен марганцевый угол тройной диаграммы [Mn, Fe]–Si–C при отношении %Mn/%Fe = = 4. Обращает внимание наличие областей существования железомарганцевых силикокарбидов [Mn, Fe]17Si4C3, [Mn,Fe]3SiC в равновесии с графитом и силикокарбида марганца Mn5Si3Cx в равновесии с SiC. Положение изотерм растворимости углерода в расплавах системы [Mn, Fe]–Si–C при %Mn/%Fe = 4 свидетельствует, что с понижением температуры равновесное содержание углерода снижается и процесс сопровождается выделением графита или карбида кремния.
Граница равновесии карбосилицидных фаз и расплавов Mn–Fe–Si–C с графитом и SiC на рис. 6.8 представлена ломанной линией.
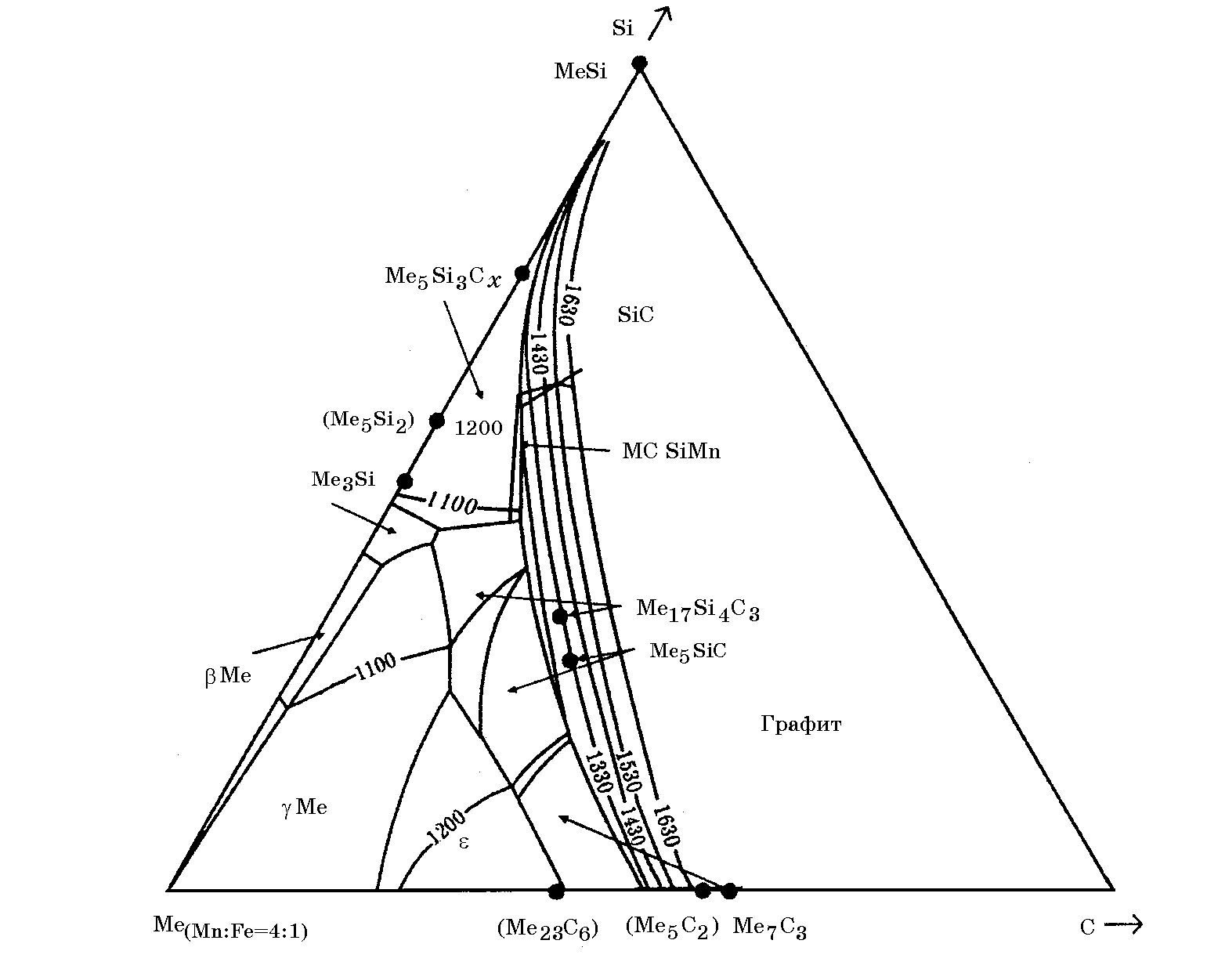
Рис.6.8. Фазовые равновесия в марганцевом углу диаграммы Ме(Mn:Fe=4:1) –Si–C с указанием областей состава сплавов в равновесии с SiC и графитом (INFACON-96); изотермы в оС
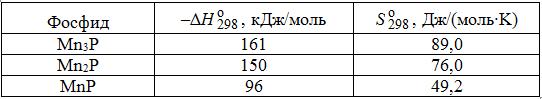
Система Mn–P (рис. 6.9). Фосфор не образует твердых растворов в марганце, но известен ряд фосфидов марганца Mn3P, Mn2P, Mn3P2 MnP (табл. 6.1).
Таблица 6.1. Энтальпия и энтропия фосфидов марганца
В расплавах системы Мn–Р имеет место сильное межчастичное взаимодействие марганца с фосфором, характеризующееся значительным отрицательным отклонением от закона Рауля.
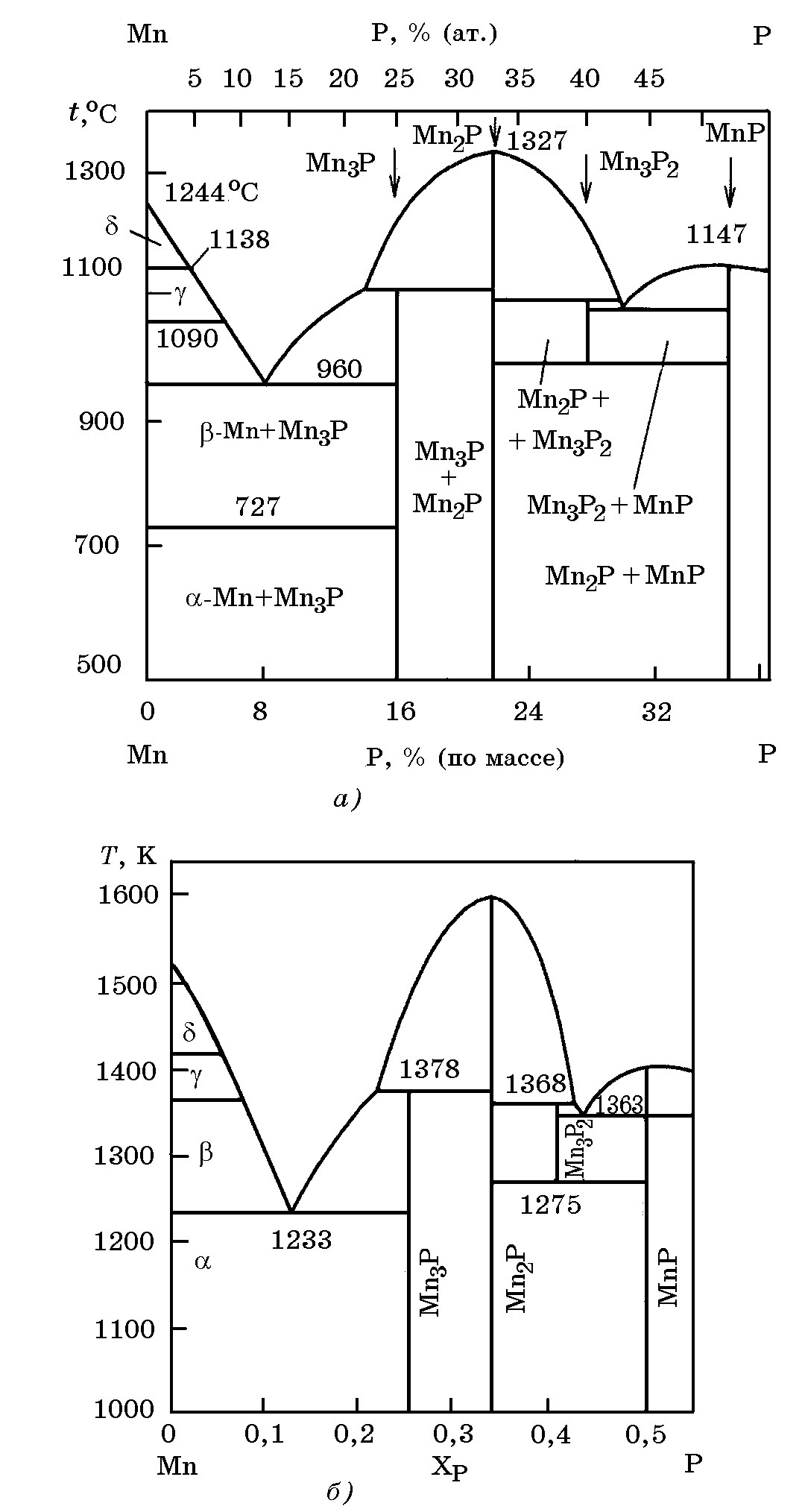
Рис. 6.9. Диаграмма равновесного состояния системы Mn–P:
а – по экспериментальным данным; б – по результатам термодинамического расчета
Система Мn–S(рис. 6.10). Марганецс серой образует термодинамически прочные сульфиды марганца MnS и MnS2. Сульфид МnS плавится при 1610оС. Изменение термодинамического потенциала реакции образования сульфида Мnт + 1/2Sт= МnSт в интервале 973–1573 K описывается выражением ∆G![]() = –296520 + 76,73Т, Дж/моль.
= –296520 + 76,73Т, Дж/моль.
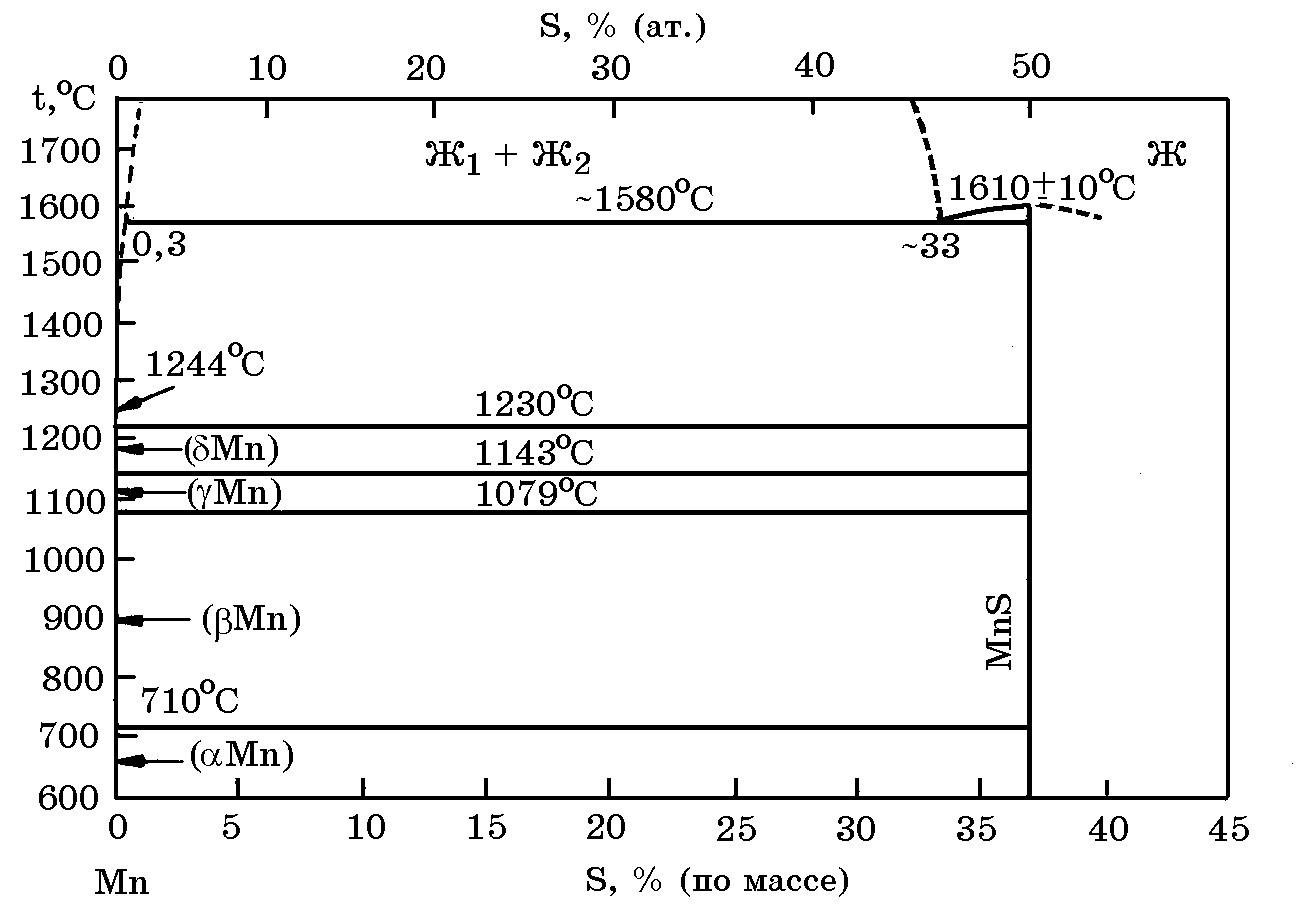
Рис. 6.10. Диаграмма равновесного состояния системы Mn–S
Система Mn–O(рис. 6.11). Уравнение для расчета растворимости кислорода в жидком марганце при аMnO = 1 имеет вид: lg[O]Mn = –4823/Т + 1,159. Эвтектике при 1245оС соответствует содержание кислорода 0,0095%.
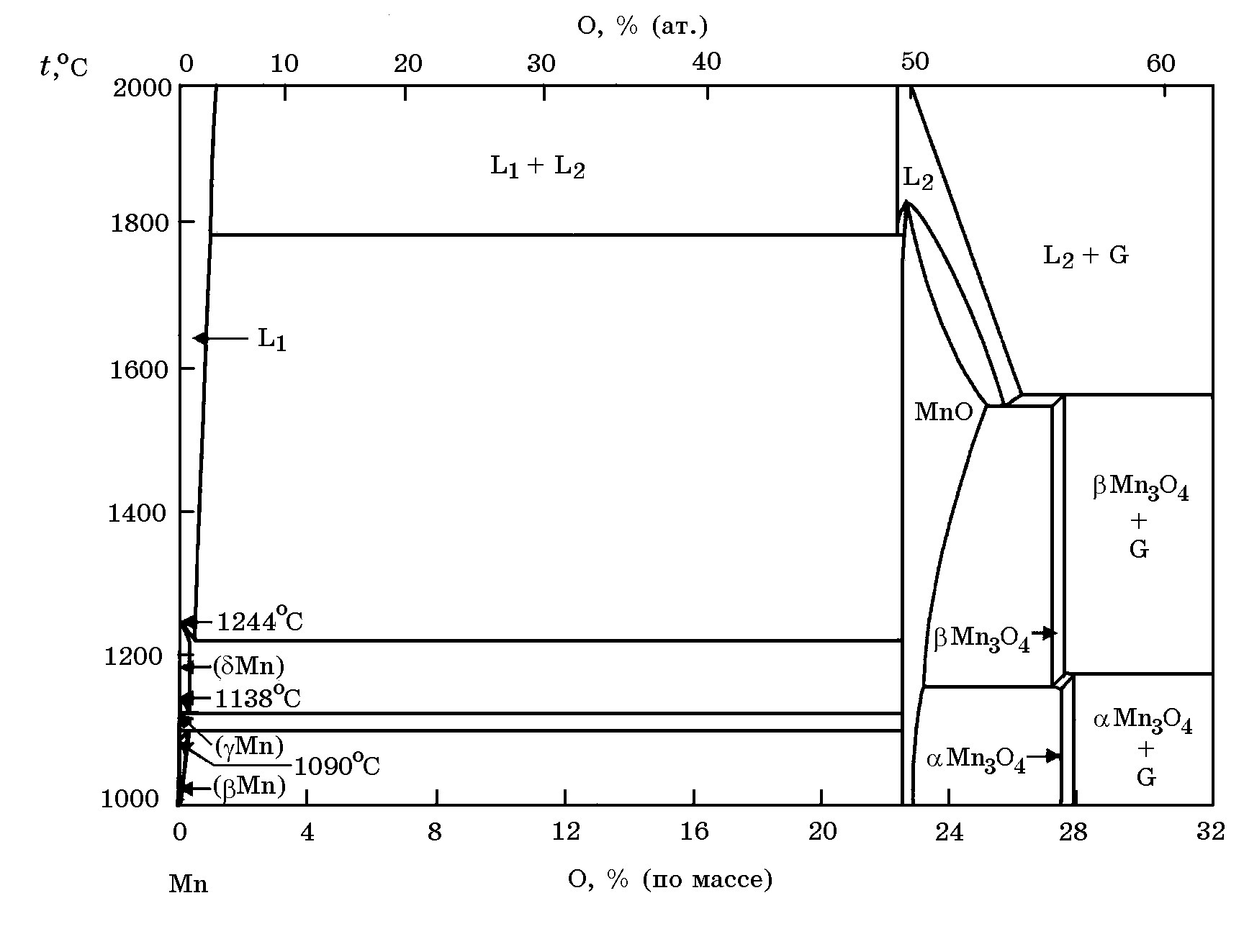
Рис. 6.11. Диаграмма равновесного состояния системы Mn–O
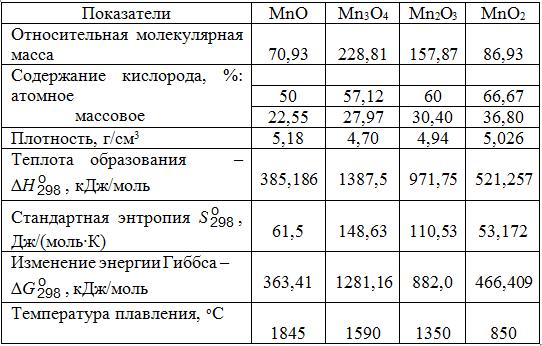
Для электрометаллургии марганца большой интерес представляет знание свойств оксидов марганца MnO2, Mn2О3, Mn3O4 и MnO (табл. 6.2).
Таблица 6.2. Физико-химические свойства оксидов марганца
Термическая диссоциация оксидов марганца. Масс-спектроскопическим методом определены давления кислорода и состав паровой фазы над MnO2, Mn2О3, Mn3O4 и MnO (табл. 6.3).
Таблица 6.3. Термодинамические данные реакций термической диссоциации кислородных соединений марганца по результатам масс-спектроскопических исследований

Термическая диссоциация низших оксидов марганца Мn3O4 и МnO происходит по реакциям 3 и 4 (см. табл. 6.3), причем давление диссоциации зависит только от температуры, так как Мn3O4 практически не имеет области гомогенности (рис.6.11).
При испарении МnО паро-газовая фаза состоит из ионов Мn+, МnО+, O+; интенсивность ионов МnO+ и О+ незначи-тельна.
Система MnO–CO2. В этой системе образуется карбонат марганца MnCO3 (родохрозит). При нагревании МnСО3 в интервале 620–690оС карбонат диссоциирует по реакции: МnCО3 = МnО + CO2. Механизм диссоциации MnСО3 сложен.
Система MnO–SiO2 (рис. 6.12). Закись марганца MnO с кремнеземом образует два соединения: тефроит (Мn2SiО4, 70,92% МnО) и родонит (МnSiO3, 54,19% МnО). Тефроит устойчив до температуры плавления 1345оС, родонит перитектически разлагается при 1291оС. В системе имеются две эвтектики, которым соответствуют температуры 1315оС и 1251оС.
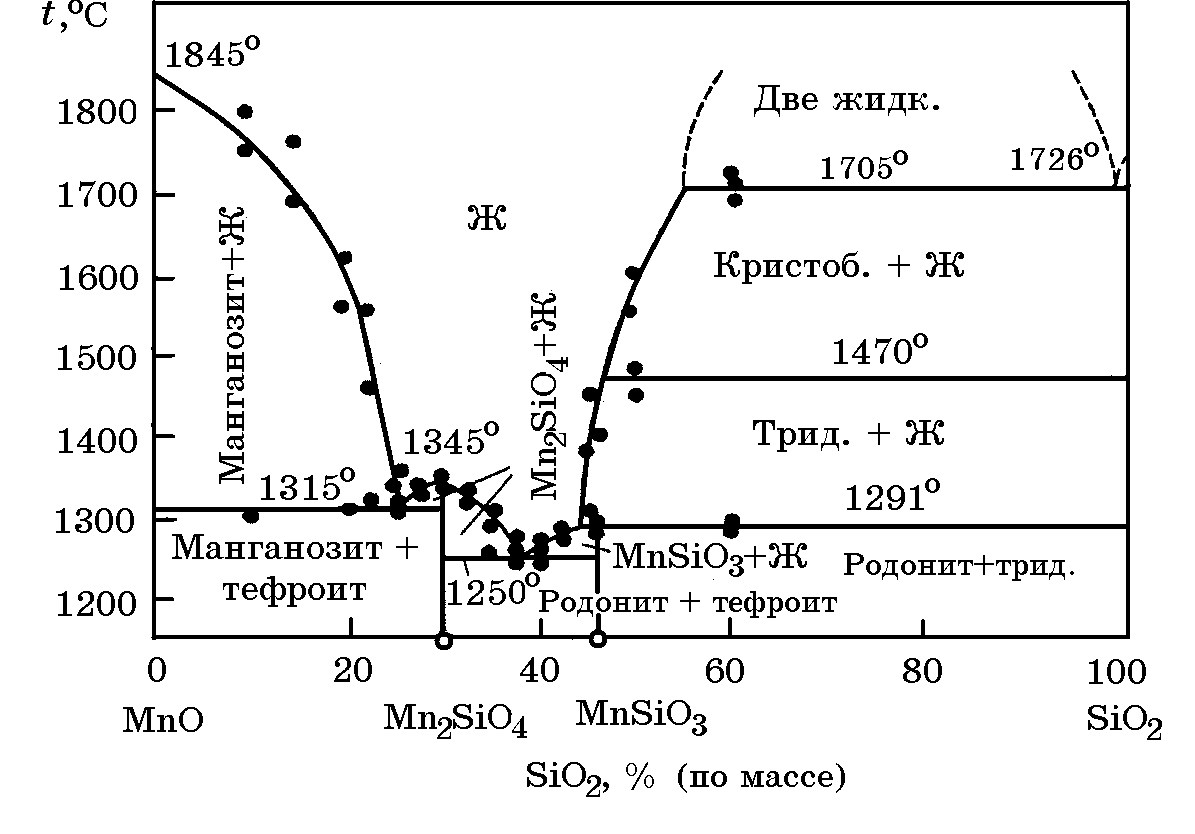
Рис. 6.12. Диаграмма равновесного состояния MnO–SiO2
Тефроит (ортосиликат) и родонит (метасиликат) образуются изоксидов по реакциям: 2MnО + SiО2 = МnSiО3, ∆Н![]() = –59440Дж/моль и МnО + SiО2 = МnSiО3 ∆Н
= –59440Дж/моль и МnО + SiО2 = МnSiО3 ∆Н![]() = –29220 Дж/моль.
= –29220 Дж/моль.
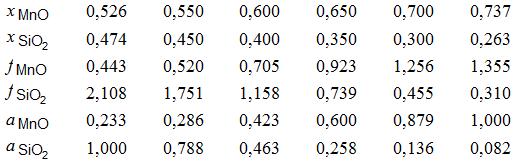
Активности MnO и SiO2 в двухфазных температурно-концентрационных областях MnО + Ж и SiO2 + Ж диаграммы состояния MnO–SiO2 (рис. 6.12) равны единице. В однофазной области существование расплава (Ж) активности MnO и SiO2 изменяются; с увеличением доли MnO ее активность увеличивается, а активность SiO2 уменьшается (рис. 6.13). при выборе в качестве стандартного состояния чистых твердых оксидов MnO и SiO2 зависимость логарифма коэффициента активности MnO и SiO2 от их мольных долей имеет вид:
lgfMnO = –3,123(1 – xMnO)2 + 0,348;
lgfSiO2 = –3,123(1 – xSiO2)2 + 1,188.
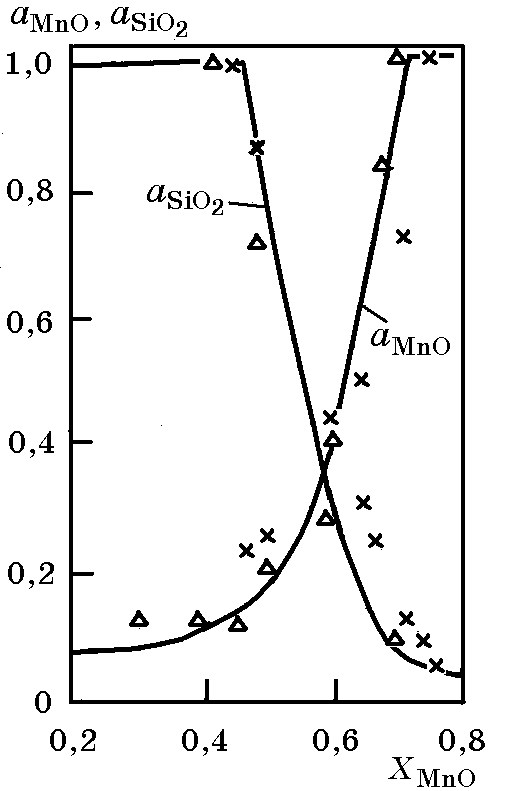
Рис. 6.13. Активность оксида марганца аMnO и кремнезема аSiO2 в системе MnO–SiO2 при 1600оС
Результаты расчетов коэффициентов активности и активности MnO и SiO2 по данным Б.П. Бурылева и Л.П. Мойсова* приведены ниже: